Лекарства
Антиретровирусные препараты
Раздел содержит краткое описание антиретровирусных препаратов, разрешенных к применению в Российской Федерации в настоящее время (дату актуализации см. в конце страниц раздела).
Описание каждого препарата состоит из следующих пунктов:
МНН — международное непатентованное название препарата, принятое Всемирной организацией здравоохранения, так же указаны принятые трехбуквенные сокращенные названия препаратов.
Торговая марка / производитель — указаны торговые марки препаратов разрешенных к применению в РФ и их производители.
Дозировки и формы выпуска — указаны дозировки и формы выпуска, зарегистрированные в РФ (если не указано иначе).
Стандартные дозы и режим приема — общая суточная доза препарата, кратность, с указанием доз и количества таблеток. Здесь и далее информация приводится в соответствии с действующими на октябрь 2009 г. рекомендациями ФНМЦ СПИД РФ, если не указано иначе.
Взаимодействия с пищей и лекарствами — указания по приему и основные взаимодействия с другими лекарственными средствами.
Наиболее значимые побочные эффекты — представленный в статье перечень побочных явлений может быть не полным, указаны лишь относительно часто возникающие или потенциально опасные побочные эффекты. Следует помнить, что указание о наличии побочных эффектов от приема препарата говорит лишь о некоторой вероятности их возникновения. Более детальную информацию о рисках, связанных с приемом лекарственных средств можно найти в соответствующих разделах сайта, а так же в специализированной литературе, (например, здесь).
Противопоказания — указаны абсолютные противопоказания, у препаратов могут быть относительные и индивидуальные противопоказания, не обсуждаемые здесь.
Внимание! Приведенная информация не может служить основанием для самостоятельного назначения или отмены препарата пациентом, самостоятельного изменения доз, кратности приема и т.п. без консультации специалиста.
Так же в разделе приводится информация о препаратах, используемых в других странах, но не зарегистрированных в России. В частности, приводится информация о лекарственных средствах, одобренных FDA* и EMA (EMEA), в США и ЕС, соответственно.
Сегодня одобрение FDA является признаком того, что новый препарат соответствует стандартам качества и прошел серьезные клинические испытания в соответствии с современными требованиями, нацеленными на безопасность и эффективность лекарственных средств.
До одобрения FDA и выхода на рынок, препарат проходит несколько этапов доклинических и клинических испытаний.
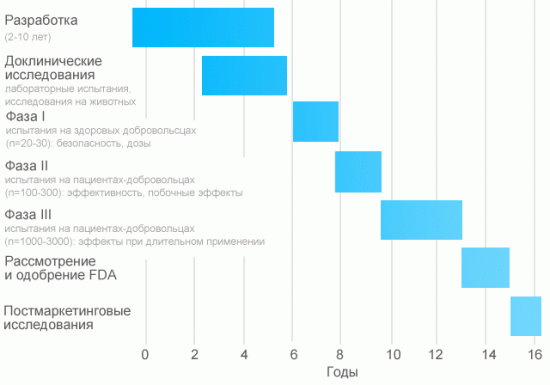
Этапы доклинических и клинических испытаний
В странах ЕС подобную FDA роль выполняет EMA (European Medicines Agency / Европейское агентство по оценке медицинских продуктов, EMEA до декабря 2009 года). ЕМЕА сравнительно молодая организация, она основана в 1977году. Многие лекарственные средства в ЕС и сегодня имеют регистрацию только национального уровня, но лекарства, появившиеся в последние два десятка лет, как правило, прошли процедуру одобрения в ЕМЕА, которая сравнима по протоколу, требованиям и срокам с процедурами FDA.
Сроки получения одобрения FDA 500 дней (180 дней для дженериков), EMA 210 дней. В настоящее время действует ускоренная система рассмотрения FDA заявок на регистрацию препарата, которая предусматривает приоритетный процесс рассмотрения безальтернативных жизненно важных препаратов. Многие антиретровирусные препараты регистрируются именно по ускоренной процедуре, которая предусматривает рассмотрение в течении полугода. Вместе с тем, общие жесткие требования FDA остаются неизменными.
* FDA (Food and Drug Administration) — Управление по контролю за качеством пищевых продуктов и лекарственных средств (США), старейшая в мире организация в области управления здравоохранением. Нормативная база FDA формировалась в результате многих происшествий и кризисов общественного доверия к безопасности лекарств, в настоящее время базируется на принципах доказательной медицины. США крупнейший в Мире потребитель и производитель лекарственных средств, и так, или иначе, все крупные мировые фармацевтические компании нацелены в первую очередь именно на рынок США, а значит и на одобрения их препаратов FDA.
Материал взят с сайта arvt.ru
Коллектив авторов arvt.ru














 Эпидситуация
Эпидситуация







